RESUMEN
Existen pocos reportes acerca de efectos epigenéticos derivados de la exposición laboral a un solo Compuesto Orgánico Volátil (COV). Tal efecto no se ha investigado en la exposición a mezclas de éstos. El objetivo fue determinar los niveles de metilación gen específica en personas expuestas ocupacionalmente a mezclas de COV. Los métodos fueron incluir a trabajadores de diferentes industrias (expuestos a COV), así como a un grupo control. Se midieron los niveles de exposición individuales a COV. Se tomaron muestras sanguíneas y se extrajo el Ácido Desoxirribonucleico (DNA, por sus siglas en inglés) para determinar, por pirosecuenciación-PCR, los niveles de metilación en 13 genes diferentes. Como resultados se encontró hipermetilación para los genes TNFα, SOD1 y TOP2A en un subgrupo expuesto. En otro subgrupo se observó hipermetilación para el gen IL6. Se pudo concluir que la exposición ocupacional a mezclas de COV tiene efectos importantes en el estado de metilación de genes involucrados con la inflamación, la reparación al DNA y el estrés oxidativo.
ABSTRACT
There are few reports about epigenetic effects in occupational exposure to a single volatile organic compound (VOC), while this same effect has not been studied in exposure to a mixture of them. In this study the levels of gene-specific methylation were determined in persons occupationally exposed to VOCs mixtures. For this study workers from different labor scenarios (exposed group to VOCs) and a reference group were included. We measured VOCs individual exposure levels. Blood samples were taken and the Deoxyribonucleic Acid (DNA) was extracted to determine, by PCR-pyrosequencing, methylation levels in 13 different genes. Hypermethylation for the TNFα, SOD1 and TOP2A genes was found in a subgroup exposed. Another exposed subgroup showed hypermethylation for the IL6 gene compared to controls. Occupational exposure to a mixture of VOCs has important effects on the methylation status of genes involved in inflammation, DNA repair and oxidative stress.
INTRODUCCIÓN
Las modificaciones epigenéticas son capaces de detectar alteraciones muy tempranas como manifestación de daño, antes de que dichas alteraciones se manifiesten como síntomas o signos clínicos (Choudhuri, Cui & Klaassen, 2010). La epigenética ha sido definida como el estudio de los cambios heredables en la expresión génica, los cuales ocurren sin cambios en la secuencia del Ácido Desoxirribonucleico (DNA, por sus siglas en inglés)(Wolffe & Guschin, 2000). Las marcas epigenéticas incluyen, pero no están limitadas a metilación del DNA modificaciones de histonas (metilación, acetilación, fosforilación, ubiquitinación, ADP-ribosilación, SUMOilación, etc.), así como Ácidos Ribonucleicos (RNA, por sus siglas en inglés) no codificantes. Los cambios epigenéticos pueden ser adquiridos en el transcurso de la vida de un individuo. Estudios recientes han demostrado que los cambios epigenéticos que son adquiridos en el ambiente intrauterino, y después del nacimiento pueden persistir a lo largo de la vida e influyen en los estados físico y mental, así como en la capacidad de confrontar el ambiente inmediato, incluyendo la capacidad para metabolizar fármacos y xenobióticos (Choudhuri et al., 2010). La evidencia creciente indica que la epigenética mantiene un potencial sustancial de desarrollar marcadores biológicos que predigan que exposiciones pondrían a las personas en riesgo y cuáles individuos de éstos que se exponen serían más susceptibles a desarrollar enfermedad (Bollati & Baccarelli, 2010). Además, las modificaciones epigenéticas representan biomarcadores más estables, al igual que huellas de exposición, comparado con la alteración génica o protéica (Jirtle & Skinner, 2007). Para el caso de la exposición a Compuestos Orgánicos Volátiles (COV), se ha reportado que la exposición laboral a benceno ha sido relacionada con modificaciones epigenéticas, específicamente metilación de DNA. A la fecha, los estudios respecto a la metilación gen específica en expuestos a benceno han mostrado hipermetilación en la región promotora de algunos genes (Bollati et al., 2007; Xing et al., 2012; 2013). Cabe mencionar que en dichos estudios se usó la misma plataforma de metilación de DNA (pirosecuenciación), en la cual, previo a un tratamiento al DNA con bisulfito, se busca cuantificar el porcentaje de metilación en la posición cinco de la base citosina, modificación que se asocia al control de la transcripción génica (Tost & Gut, 2007). Hasta ahora, no se ha estudiado si la exposición laboral a tolueno, xileno, n-hexano, o bien, a una mezcla de estos compuestos, tenga algún efecto sobre la metilación al DNA, ya sea global o a nivel gen-específico. Con base en lo anterior, el objetivo de este trabajo fue determinar los niveles de metilación en la región promotora de genes involucrados en las vías celulares de inflamación, reparación de DNA, estrés oxidativo y metabolismo de xenobióticos, en personas expuestas ocupacionalmente a un solo COV o a mezclas de ellos.
MATERIALES Y MÉTODOS
a) Participantes. Después de la invitación y firma del consentimiento informado, se incluyeron a 206 trabajadores, quienes se dividieron en diferentes grupos, a saber: i) trabajadores de la industria de la curtiduría (n = 24); ii) trabajadores de una fábrica de calzado de piel (n = 40); iii) trabajadores de una gasolinera (n = 36); iv) trabajadores de una fábrica de calzado de plástico (n = 40); y v) trabajadores administrativos de dos universidades (n = 66, grupo control o de referencia, sin exposición laboral a COV).
b) Medición de los niveles individuales de exposición a COV. Se colocó un difusor pasivo de carbono (Supelco, Sigma-Aldrich Co., St. Louis MO) en la solapa de los trabajadores durante una jornada laboral de 8 h. Se separó el tubo de carbono activado, al cual se le aplicó disulfuro de carbono para su desorción. Una vez pretratadas las muestras, se realizó la lectura en un cromatógrafo de gases acoplado a espetrometría de masas (GC/MS, Perkin Elmer, Modelo Clarus 600, Waltham, MA, EUA). A los trabajadores de la curtiduría se les midieron sólo tres COV: benceno, tolueno y etilbenceno; al resto, además de los tres anteriores, se les midieron niveles de acetona, metil etil cetona, n-hexano y xileno.
c) Datos sociodemográficos y obtención de muestra. Después de realizarles una encuesta de salud, la cual incluía preguntas acerca de datos sociodemográficos, antecedentes patológicos y de consumo de drogas ilegales, y previa firma del consentimiento informado, se les tomó a cada participante una muestra de sangre venosa del brazo (aproximadamente 15 ml), divididas en cuatro tubos, los cuales se almacenaron a -80 ºC.
d) Aislamiento del DNA. Previa descongelación paulatina, se separó el DNA de cada muestra de sangre completa de los participantes, de acuerdo con las recomendaciones del fabricante del kit DNAeasy Extraction Kit (Qiagen, Valencia, CA, USA). Después de la extracción del DNA, su concentración en la elución final fue cuantificada. El DNA eluido fue almacenado hasta su uso a -80 ºC.
e) Diseño y obtención de las secuencias de la región promotora de los genes de interés. Con el objeto de estudiar la metilación de una región específica del DNA (en este caso, la región promotora de los genes de interés), se realizó el diseño de las secuencias tomando en cuenta la descripción de éstas (en artículos científicos o en recursos web), corroborando si dichas secuencias pertenecían a la región y gen de interés a través del recurso web de la Universidad de California en Santa Cruz (http://genome.ucsc.edu/). Una vez obtenidas las secuencias, se procedió al diseño de la región cebadora (primer), simulando el tratamiento con bisulfito de dicha región. Esto se logró gracias al recurso web de la Universidad de California en San Francisco denominado methprimer. Se diseñaron los primers para 13 genes, agrupados de acuerdo con la vía celular de interés: inflamación (TNFα, IL6, iNOS, COX-2), estrés oxidativo (HMOX-1, GSTM1, GSTP1, SOD1), reparación al DNA (p53, WRAP53, RAD51, TOP2A) y metabolismo de xenobióticos (CYP2E1). Una vez diseñadas las secuencias se ordenaron al fabricante, quien envió tres primers para cada gen (uno de avance, uno de reversa y otro de secuenciación) en presentación de liofilizado. Los primers se diluyeron con agua libre de DNAsas y RNAasas, y se almacenaron a -20 ºC. Se obtuvieron primers de secuenciación con un número de repetidos CG de 1 a 10.
f) Tratamiento del DNA con bisulfito. El DNA genómico obtenido en el inciso d fue tratado con bisulfito con el kit EZ-DNA Methylation Gold para 96 pozos. El objetivo de este tratamiento es convertir todas las citosinas no metiladas del DNA a uracilos.
g) Reacción en Cadena de la Polimerasa (PCR, por sus siglas en inglés). Una vez tratado con bisulfito y previamente identificado, el DNA de los participantes se mezcló con los primers de avance y reversa obtenidos en el inciso e, a los cuales además se les agregó una DNA polimerasa comercial (Taq Polymerase). Previas pruebas de temperatura de templado para cada gen, se sometieron las placas de 96 pozos a diferentes temperaturas, por medio de un termociclador para permitir las reacciones.
h) Pirosecuenciación. Cada placa donde se realizó la PCR fue pretratada con esferas de sefarosa, y asimismo se le adicionó el primer de secuenciación. Se prepararon duplicados de cada placa, los cuales fueron procesados por el equipo Pyromark 96 MD (Qiagen, Valencia, CA, USA). El pirosecuenciador, a través de una reacción que emite una señal luminosa, nos da al final el porcentaje de metilación en la región de interés, donde se ubican los repetidos citosina-guanina (repetidos CG; Tost & Gut, 2007).
i) Análisis estadístico. Los resultados de metilación entre duplicados fueron contrastados por medio de la prueba de regresión lineal simple. Se descartaron aquellos resultados donde se obtuvo un coeficiente de relación Pearson menor a 0.3. Después de aplicar este criterio, al menos uno repetido CG fue analizado en 9 de los 13 genes en los que se realizó la PCR. Para determinar las diferencias de metilación entre grupos, tomando en cuenta si en las personas que lo conformaron hubo diferencias en cuanto a género, edad y hábito de fumar, se diseñó un modelo de regresión lineal con covariables. Se consideraron los resultados con diferencia estadísticamente significativa a aquéllos con un valor de p menor a 0.05.
RESULTADOS
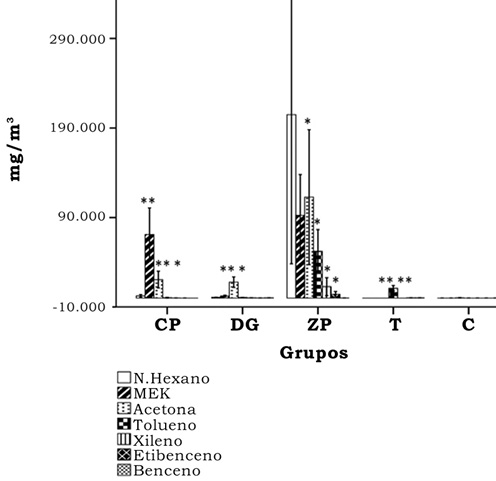
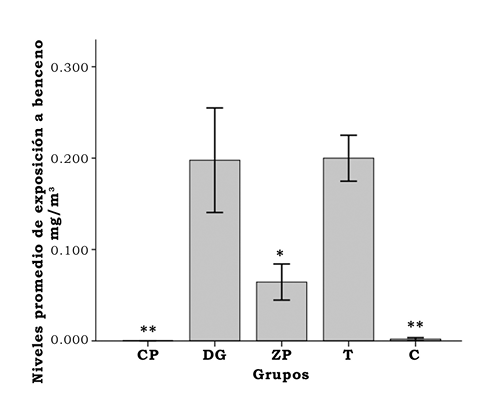
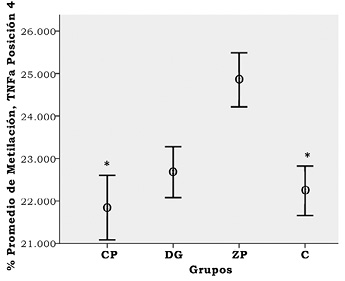
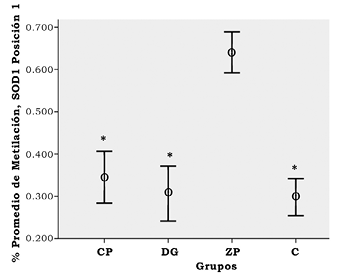
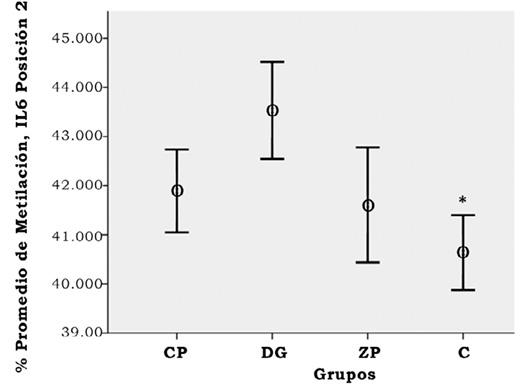
En la figura 1 se resumen los resultados de los niveles individuales de los COV obtenidos en los diferentes lugares de trabajo. Es importante mencionar que en las tenerías sólo se midieron niveles de benceno, etilbenceno y tolueno, de los cuales se encontraron mayores niveles de tolueno en las tenerías en comparación con el control (p < 0.001). El resto de los COV medidos en los demás escenarios laborales se encontraron en mayores concentraciones comparados con el grupo control, a excepción del benceno en trabajadores de la fábrica de calzado de plástico (CP), lugar donde los valores arrojaron cero absoluto. En cuanto a las diferencias entre los lugares de trabajo, el tolueno fue mayor en las tenerías con respecto a despachadores de gasolina (DG) y CP. La metiletilcetona fue el compuesto que se presentó con mayores niveles en CP, sin diferencia significativa con trabajadores de la fábrica de calzado de piel (ZP). Para ZP comparado con DG, el tolueno, la acetona, metiletilcetona (MEK) y los xilenos fueron mayores en la fábrica de calzado (p < 0.001), mientras que los niveles individuales de benceno y el metiletilacetato fueron mayores en la estación de gasolina (p = 0.007/ p < 0.001, respectivamente). Debido a los altos niveles de n-hexano y otros compuestos, la escala de la figura 1 no permite apreciar las diferencias entre los niveles de benceno, por lo que éstos se muestran por separado en la figura 2. En cuanto a los resultados de metilación gen-específica, sólo fue posible obtener resultados confiables (de acuerdo con el bajo valor del coeficiente de correlación de Pearson entre duplicados) para 9 de los 13 genes para los que se realizó la pirosecuenciación-PCR. Los cuatro genes, cuya información no fue analizada, fueron WRAP53, RAD51, p53 y GSTM1. Al hacer el análisis de regresión lineal con covariables se observaron mayores niveles de metilación (p < 0.05-0.001) para tres genes en los trabajadores de ZP: TNFα en el sitio de metilación cuatro (figura 3), SOD1 en un sitio de metilación (figura 4) y TOP2A en un sitio de metilación (figura 5). En el caso de los trabajadores de DG, el promotor del gen de IL6 en su sitio de metilación núm. 2 presentó mayores niveles de comparado con el grupo control (figura 6).
|
| |
 |
| |
Figura 1. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia. |
 |
Figura 1. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia.. Close |
|
| |
 |
| |
Figura 2. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia. |
 |
Figura 2. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia.. Close |
|
| |
 |
| |
Figura 3. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia. |
 |
Figura 3. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia.. Close |
|
| |
 |
| |
Figura 4. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia. |
 |
Figura 4. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia.. Close |
|
| |
 |
| |
Figura 5. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia. |
 |
Figura 5. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia.. Close |
|
| |
 |
| |
Figura 6. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia. |
 |
Figura 6. Riesgos estratégicos (internos y externos).
Fuente: Elaboración propia.. Close |
DISCUSIÓN
En este trabajo se observó que la mayor cantidad de genes que mostraron hipermetilación fueron los correspondientes a los trabajadores de ZP, grupo de personas expuestas a los más altos niveles de hasta cinco COV. A la fecha, no hay datos referentes a los efectos epigenéticos derivados de la exposición concurrente a mezclas de compuestos con potencial tóxico. Sin embargo, sí podemos contrastar nuestros resultados con respecto a lo que se ha publicado en cuanto a la exposición a un solo COV y sus efectos sobre la metilación del DNA: los trabajadores de DG presentaron mayores niveles de exposición a benceno con respecto a todos los demás grupos de exposición (p < 0.005-0.001) (figura 3) y mostraron hipermetilación en el gen IL6, lo cual concuerda con la hipermetilación observada para el gen p15 en trabajadores expuestos a benceno (Bollati et al., 2007), así como con la hipermetilación en los genes p16 (Xing et al., 2012) y ERCC3 (Xing et al., 2013) en trabajadores expuestos al mismo compuesto. Cabe mencionar que los estudios de metilación al DNA mencionados anteriormente fueron realizados, al igual que en el presente trabajo, en leucocitos de las personas expuestas. Por otro lado, a la fecha no hay datos respecto al efecto de la metilación del DNA como resultado de la exposición única a acetona, etilbenceno, tolueno y metiletilcetona, los cuales presentaron altos niveles en los trabajadores de ZP. Sin embargo, para n-hexano, compuesto que presentó los mayores niveles de exposición en este escenario laboral, existen datos, en un modelo de exposición animal por inhalación, que muestran que la exposición in utero a este compuesto en ratas causó hipermetilación de hasta cinco genes relacionados con vías apoptóticas y de síntesis de hormonas en la progenie (Li et al., 2014), lo cual coincide en cierta medida con nuestros resultados.